
科目: 来源: 题型:
在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g) 1/2N2(g)+CO2(g);ΔH=-373.2 kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
1/2N2(g)+CO2(g);ΔH=-373.2 kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
A 加催化剂同时升高温度 B 加催化剂同时增大压强
C 升高温度同时充入N2 D 降低温度同时增大压强
查看答案和解析>>
科目: 来源: 题型:
将a g块状碳酸钙跟足量盐酸反应,反应物损失的质量随时间的变化曲线如下图的实线所示。在相同的条件下,将b g(a>b)粉末状碳酸钙与同浓度盐酸反应,则相应的曲线(图中虚线所示)正确的是( )




查看答案和解析>>
科目: 来源: 题型:
已知反应:①101kPa时,2C(s)+O2(g)==2CO(g);ΔH=-221 kJ/mol
②稀溶液中,H+(aq)+OHˉ(aq)==H2O(l);ΔH=-57.3 kJ/mol
下列结论正确的是
A.碳的燃烧热大于110.5 kJ/mol
B.①的反应热为221 kJ/mol
C.稀硫酸与稀Ba(OH) 2溶液反应的中和热为-57.3 kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量
查看答案和解析>>
科目: 来源: 题型:
在25℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,下列热化学方程式正确的是( )
A.CH3OH(l)+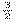 O2(g)===CO2(g)+2H2O(l);ΔH=+725.8 kJ/mol
O2(g)===CO2(g)+2H2O(l);ΔH=+725.8 kJ/mol
B.2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l);ΔH=-1452 kJ/mol
C.2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l);ΔH=-725.8 kJ/mol
D.2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l);ΔH=+1452 kJ/mol
查看答案和解析>>
科目: 来源: 题型:
某溶液中含有Ba2+,Cu2+, Ag+,现用NaOH溶液、
盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。
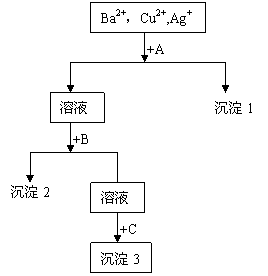
其流程图如右所示(写出最佳答案)
(1).沉淀的化学式:
沉淀1 ,
沉淀2 ,
沉淀3 ;
(2).写出混合液+A的离子方程式:
。
溶液+B的离子方程式:
。
查看答案和解析>>
科目: 来源: 题型:
实验室通常用MnO2和浓盐酸共热制取Cl2,反应的化学方程式为
MnO2 + 4HCl(浓) 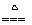 MnCl2 + Cl2↑+ 2H2O。
MnCl2 + Cl2↑+ 2H2O。
(1)该反应的氧化剂是 ,氧化产物是 ,用单线桥法表示上述反应电子转移方向和数目。
(2)计算当有73.0克HCl完全参加反时,消耗MnO2的物质的量为多少?
生成的气体在标准状况下的体积多少升?
查看答案和解析>>
科目: 来源: 题型:
实验室配制100mL 0.5mol·L-1的NaOH溶液,有如下操作步骤:
①把称量好的NaOH固体放入小烧杯中,加适量蒸馏水溶解;
②把①所得溶液待冷却至室温后,用玻璃棒引流小心转入100mL容量瓶中;
③继续向容量瓶中加蒸馏水至液面距离刻度l—2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部,与刻度线相切;
④用少量蒸馏水洗涤烧杯和玻璃棒2—3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀;
⑤将容量瓶塞紧,充分摇匀。
请填写下列空白:
(1).配制前,应先用托盘天平准确称取NaOH固体 克;
(2).上述实验操作步骤的正确顺序为(填序号) ;
(3).本实验用到的容量瓶上无需标记的是 ;
A.温度 B.刻度线 C.浓度 D.容积
(4).若实验过程中出现如下情况如何处理?
加蒸馏水时不慎超过了刻度 。
查看答案和解析>>
科目: 来源: 题型:
(1)向某溶液中加入KSCN溶液无明显现象,再滴入数滴氯水后,溶液立即变成红色,则原溶液中一定含有________离子,要除去FeCl3溶液中少量的氯化亚铁,可行的办法是________(填字母)。
A.加入铜粉 B.加入铁粉 C.通入氯气 D.加入KSCN溶液
根据选用的试剂,写出除去FeCl3溶液中少量的氯化亚铁过程中发生反应的离子方程式
________________________ _______。
(2)电子工业常用30%的FeCl3溶液腐蚀铜箔,制造印刷线路板,写出FeCl3与金属铜反应的离子方程式____________ __________________________。
(3)使用过的腐蚀液会失效,但可以回收利用,某兴趣小组为了从使用过的腐蚀液中回收铜,应使用的试剂是________(填字母)。
A.铜粉 B.氯气 C.铁粉 D.KSCN溶液
(4)向沸水中逐滴滴加1 mol·L-1FeCl3溶液至液体呈透明的红褐色,该分散系中微粒直径的范围是
___ ______nm,区别该液体和FeCl3溶液可用 方法。
查看答案和解析>>
科目: 来源: 题型:
某蓝色电解质溶液中,只可能大量存在有Ag+、H+、Cu2+、CO32—、OH—、Cl—中的某些离子,你认为一定有的离子是 ,一定没有的离是 ,还需进一步确认的是 。
查看答案和解析>>
科目: 来源: 题型:
阅读下列材料后回答问题:一个体重50Kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+还原成Fe2+,有利于人体吸收。
(1)在人体中进行Fe2+ 的转化时,实现①的转化需消耗 剂(填氧化或还原),

Fe3+
通常用 (填试剂名称)检验Fe3+存在。
(2)“服用维生素C,可使食物中的Fe3+还原成Fe2+”这句话指出,维生素C在这一反应中作 剂,Fe3+发生 反应。
(3)市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成亚铁盐。此反应的离子方程式为
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com