

科目: 来源: 题型:
【题目】有Fe、H2、Ba(OH)2溶液,K2CO3溶液,NaOH溶液,稀硫酸等六种物质,在常温下两种物质间能发生的化学反应最多有
A. 4个 B. 5个 C. 6个 D. 7个
查看答案和解析>>
科目: 来源: 题型:
【题目】对于可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A. 化学平衡常数的表达式K=![]()
B. 当v正(NH3)∶v正(NO)=1∶1时,说明该化学反应已经达到平衡状态
C. 若达到平衡状态时两种反应物的转化率相等,则起始投入时n(NH3)∶n(O2)=4∶5
D. 反应达到平衡状态后,改变条件平衡使平衡向正反应方向移动,c(H2O)一定增大
查看答案和解析>>
科目: 来源: 题型:
【题目】三硫化四磷用于制造火柴即火柴盒摩擦面,分子结构如图所示。下列有关三硫化四磷的说法正确的是( )
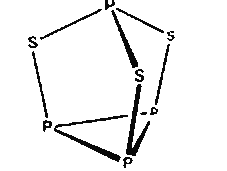
A. 该物质中磷元素的化合价为+3
B. 22 g P4S3含硫原子数目约为1.806×1023
C. 该物质分子结构中S、P最外层电子数均不为8
D. 该物质分子中全是极性共价键
查看答案和解析>>
科目: 来源: 题型:
【题目】可逆反应2SO2+O2![]() 2SO3,正反应速率分别用v(SO2)、v(O2)、v(SO3)(mol·L-1·min-1)表示,逆反应速率分别用v′(SO2)、v′(O2)、v′(SO3)(mol·L-1·min-1)表示,当反应达到化学平衡时,正确的关系是( )
2SO3,正反应速率分别用v(SO2)、v(O2)、v(SO3)(mol·L-1·min-1)表示,逆反应速率分别用v′(SO2)、v′(O2)、v′(SO3)(mol·L-1·min-1)表示,当反应达到化学平衡时,正确的关系是( )
①v(SO2)=v′(SO2) ②v(O2)=v′(SO2)=v(SO3)
③v(O2)=![]() v′(SO2) ④v′(SO2)=v′(O2)=v′(SO3)
v′(SO2) ④v′(SO2)=v′(O2)=v′(SO3)
A. ①②③④B. ①②③C. ②③④D. ①③
查看答案和解析>>
科目: 来源: 题型:
【题目】NA为阿伏伽德罗常数,下列叙述正确的是( )
A. 1L 1mol·L-1盐酸所含的氯化氢分子数为NA B. 2.24LSO3中含有分子数为0.1NA
C. 0.1 mol Fe与足量稀HNO3反应转移电子数为0.3NA D. 7.8 g Na2O2中含有的阴离子数目为0.2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】在1L定容的密闭容器中,可以证明可逆反应N2+3H2![]() 2NH3已达到平衡状态的是
2NH3已达到平衡状态的是
A. c(N2):c(H2):c(NH3)=1:3:2
B. 一个N≡N 断裂的同时,有3个H-H生成
C. 其他条件不变时,混合气体的密度不再改变
D. v正(N2)═2 v逆(NH3)
查看答案和解析>>
科目: 来源: 题型:
【题目】容积固定的密闭容器中,达平衡的可逆反应2A(g)![]() 2B(?) + C (?)(△H>0),若随着温度升高,气体平均相对分子质量减小,则下列判断正确的是:( )
2B(?) + C (?)(△H>0),若随着温度升高,气体平均相对分子质量减小,则下列判断正确的是:( )
A. B和C可能都是液体 B. B和C肯定都是气体
C. B和C可能都是固体 D. 若C为固体,则B一定是气体。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化铜、氯化亚铜是重要的化工原料,广泛地用作有机合成催化剂。
I.实验室中以粗铜(含杂质Fe)为原料制备铜的氯化物。现用如图所示的实验仪器及药品来制备纯净、干燥的氯气并与粗铜反应(铁架台、铁夹、酒精灯已省略)。按要求回答下列问题:
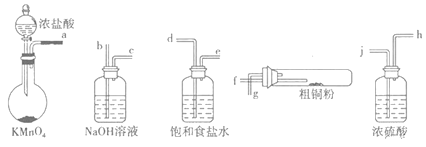
(1)按气流方向连接各仪器接口顺序是:a![]() ______________________________。
______________________________。
(2)写出加热时硬质试管中发生化学反应的方程式是______________________________。
(3)反应后,盛有NaOH溶液的广口瓶中溶液具有漂白、消毒作用,若用钢铁(含Fe、C)制品盛装该溶液会发生电化腐蚀,钢铁制品表面生成红褐色沉淀,溶液会失去漂白、杀菌消毒功效。该电化腐蚀过程中正极反应式是_______________________________。
II.将上述实验制得的固体产物按如下流程操作,试回答下列问题:
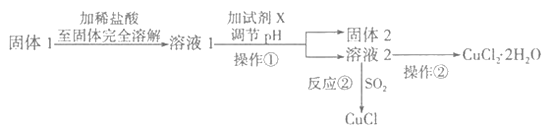
(1)检验溶液2中是否含有杂质离子的试剂是__________________。
(2)某同学用实验制得的CuCl2·2H2O晶体配制500mL0.1 mol·L-1的CuCl2溶液,在称量出CuCl2·2H2O晶体后,溶解该晶体的具体操作为_________________________________,分析以下操作对配制的溶液浓度造成的影响,影响偏高的是___________________________。
①蒸馏水洗完容量瓶后没有烘干 ②转移溶液过程中出现漏液
③砝码生锈 ④定容时俯视
(3)溶液l可加试剂X用于调节pH以除去杂质,X可选用下列试剂中的(填序号)_________。
a.NaOH b.NH3·H2O c.CuO d.CuSO4 e.Cu2(OH)2CO3
(4)反应②是向溶液2中通入一定量的SO2,加热一段时间后生成CuCl白色沉淀。写出制备CuCl的离子方程式:_________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某可逆反应mA(g)+nB(g)![]() pC(g)在密闭容器中进行,右图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是
pC(g)在密闭容器中进行,右图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是
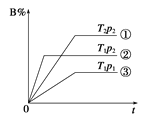
A.T1<T2 p1>p2 m+n>p 放热反应
B.T1>T2 p1<p2 m+n>p 吸热反应
C.T1<T2 p1>p2 m+n<p 放热反应
D.T1>T2 p1<p2 m+n<p 吸热反应
查看答案和解析>>
科目: 来源: 题型:
【题目】按反应N2H5++4Fe3+……→4Fe2++Y+……,在水溶液中N2H5+离子将Fe3+还原为Fe2+,作为N2H5+离子的氧化产物Y可能为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com