
科目: 来源: 题型:选择题
| A. | H2(g)+ O2(g)═H2O(g)△H=+242 kJ/mol | B. | 2H2(g)+O2(g)═2H2O(l)△H=-484kJ/mol | ||
| C. | H2(g)+ O2(g)═H2O(g)△H=-242kJ/mol | D. | 2H2(g)+O2(g)═2H2O(g)△H=+484 kJ/mol |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 苯中溶有苯酚(浓溴水,过滤) | B. | 甲烷中含有乙烯(溴水,洗气) | ||
| C. | 乙醇中的乙酸(NaOH溶液,分液) | D. | 乙醇中含有水(金属钠,蒸馏) |
查看答案和解析>>
科目: 来源: 题型:解答题
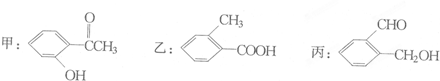
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 甘油 | B. | 甲醇 | C. | 乙醇 | D. | 乙二醇 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
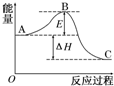 2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H=-99 kJ•mol-1.请回答下列问题:
2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H=-99 kJ•mol-1.请回答下列问题:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CxHy(l)+(x+)O2(g)═xCO2(g)+H2O(l)△H=(-Q+23.5)kJ•mol-1 | |
| B. | CxHy(l)+( x+)O2═xCO2+H2O(l)△H=?-?kJ•mol-1 | |
| C. | CxHy(l)+(x+)O2(g)═xCO2(g)+H2O(l)△H=- kJ•mol-1 | |
| D. | CxHy(l)+( x+)O2(g)═xCO2(g)+H2O(l)△H=(-+2.61)kJ•mol-1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CH4 (g)+2O2(g)═CO2 (g)+2H2O(l)△H=a kJ•mol-1 CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=b kJ•mol-1 | |
| B. | 2H2(g)+O2(g)═2H2O(l)△H=a kJ•mol-1 H2(g)+O2(g)═H2O(l)△H=b kJ•mol-1 | |
| C. | C(s)+O2 (g)═CO(g)△H=a kJ•mol-1 C(s)+O2(g)═CO2(g)△H=b kJ•mol-1 | |
| D. | S(g)+O2(g)═SO2 (g)△H=a kJ•mol-1 S(s)+O2(g)═SO2(g)△H=b kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com