
科目: 来源: 题型:选择题
| A. | 2Na2O2+2H2O═4NaOH | |
| B. | 2S+3O2═2SO3 | |
| C. | 3NO2+2H2O═3HNO3 | |
| D. | MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2Na+2H2O═2NaOH+H2↑ | B. | SiO2+H2O═H2SiO3 | ||
| C. | Cl2+2NaOH═NaCl+NaClO+H2O | D. | 2H2S+SO2═3S+2H2O |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2H2+O2=2H2O,△H=-484kJ/mol | B. | H2O(g)=H2(g)+O2(g)△H=+242kJ/mol | ||
| C. | 2H2(g)+O2(g)=2H2O(l),△H=-484kJ/mol | D. | H2(g)+O2(g)=H2O(g)△H=+242kJ/mol |
查看答案和解析>>
科目: 来源: 题型:解答题
 △H=+88.6kJ•mol-1则M、N相比,较稳定的是M.
△H=+88.6kJ•mol-1则M、N相比,较稳定的是M.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
 纯醋酸中不断加入水后,导电能力与加水量的关系如图,请回答有关a、b、c三个点表示的问题:
纯醋酸中不断加入水后,导电能力与加水量的关系如图,请回答有关a、b、c三个点表示的问题:查看答案和解析>>
科目: 来源: 题型:选择题
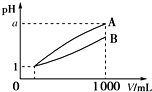 pH=1的两种酸溶液A、B各1mL,分别加水稀释到1 000mL,其pH与溶液体积(V)的关系如图所示,下列说法不正确的是( )
pH=1的两种酸溶液A、B各1mL,分别加水稀释到1 000mL,其pH与溶液体积(V)的关系如图所示,下列说法不正确的是( )| A. | 若a=4,则A是强酸,B是弱酸 | |
| B. | 稀释后,A酸溶液的酸性比B酸溶液强 | |
| C. | A、B两种酸溶液的物质的量浓度一定不相等 | |
| D. | 若1<a<4,则A、B都是弱酸 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 通入HCl | B. | 加少量NaOH固体 | C. | 加水 | D. | 升温 |
查看答案和解析>>
科目: 来源: 题型:填空题
| Fe3+ | Al3+ | Fe2+ | Mg2+ | |
| 开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
| 沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com