
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1352 | B. | 1456 | C. | 496 | D. | 360 |
查看答案和解析>>
科目: 来源: 题型:填空题
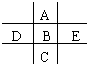 如图为周期表的一小部分,A、B、C、D、E的位置关系如图所示.其中B元素的最高正价是最低负价绝对值的3倍,它的最高氧化物中含氧60%,回答下列问题:
如图为周期表的一小部分,A、B、C、D、E的位置关系如图所示.其中B元素的最高正价是最低负价绝对值的3倍,它的最高氧化物中含氧60%,回答下列问题: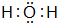 .
.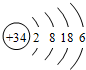 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Ba(OH)2•8H2O+2NH4Cl=BaCl2•6H2O+2NH3•2H2O+2H2O | |
| B. | Ba(OH)2+H2SO4=BaSO4↓+2H2O | |
| C. | 2Al+2NaOH+2H2O=2NaAlO2+3H2↑ | |
| D. | 8Al+3Fe3O4=4Al2O3+9Fe |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 把一段打磨过镁带放入冷水中 | B. | 把铝条放入NaOH溶液中 | ||
| C. | 把绿豆大的钠投入到KCl溶液中 | D. | 把溴水滴加到淀粉KI溶液中 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 铍原子失电子的能力比钙弱 | B. | 砹的氢化物不如碘化氢稳定 | ||
| C. | 硒酸的酸性比硫酸强 | D. | 氢氧化锶的碱性比氢氧化钙强 |
查看答案和解析>>
科目: 来源: 题型:解答题
 汽车尾气中含有NO、CO和碳颗粒等有害物质,已成为某些大城市空气的主要污染源.
汽车尾气中含有NO、CO和碳颗粒等有害物质,已成为某些大城市空气的主要污染源. 2NO;汽车启动后,汽缸内温度越高,单位时间内NO排放量越大,试分析其原因温度升高,反应速率加快.
2NO;汽车启动后,汽缸内温度越高,单位时间内NO排放量越大,试分析其原因温度升高,反应速率加快.查看答案和解析>>
科目: 来源: 题型:解答题
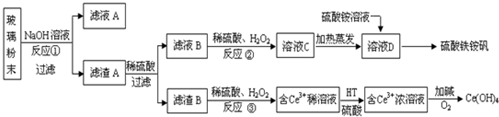
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 钠是密度小、硬度大、熔点高的银白色金属 | |
| B. | 钠在纯净的氧气中充分燃烧,生成白色固体Na2O | |
| C. | 将金属钠放入CuSO4溶液中,可观察到大量红色的铜析出 | |
| D. | 将金属钠放入水中立即熔化成小球,说明金属钠熔点低,且反应放出热量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com