
科目: 来源: 题型:选择题
| A. | c(OH-)=c(Na+)+c(H+) | |
| B. | 该溶液中的c(OH-)=1.0×10-3mol•L-1 | |
| C. | 加水稀释104倍所得溶液显碱性 | |
| D. | 与pH=3的HF溶液等体积混合所得溶液:c(Na+)=c(F-)+c(HF) |
查看答案和解析>>
科目: 来源: 题型:解答题
 .
.
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 2CN-+Cl2→(CN)2+2Cl- | B. | (CN)2+H2O→2H++CN-+CNO- | ||
| C. | (CN)2+2OH-→CN-+CNO-+H2O | D. | (SCN)2+2CN-→2SCN-+(CN)2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NaHSO4溶液与Ba(OH)2溶液反应 | B. | C6H5ONa溶液与CO2反应 | ||
| C. | NaAlO2溶液与CO2反应 | D. | Fe与稀硝酸反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中下图是己经合成的最著名的硫-氮化合物的分子结构.有关该物质说法错误的是( )
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中下图是己经合成的最著名的硫-氮化合物的分子结构.有关该物质说法错误的是( )| A. | 分子式为S4N4 | B. | 分子中既有极性键又有非极性键 | ||
| C. | 熔点低于同类晶体S2N2 | D. | 熔沸点低,硬度较小 |
查看答案和解析>>
科目: 来源: 题型:解答题

 溶液出现蓝色且30s内不褪色
溶液出现蓝色且30s内不褪色查看答案和解析>>
科目: 来源: 题型:解答题
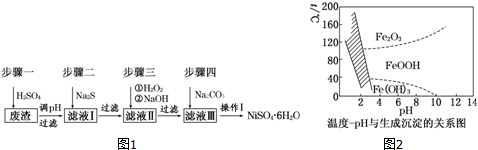
查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:填空题
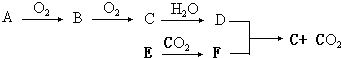
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com