

科目: 来源: 题型:选择题
| A. |  的系统命名:2-丙醇 的系统命名:2-丙醇 | B. | 明矾的化学式:KAl(SO4)2•12H2O | ||
| C. | CH4Si的结构式: | D. | H2O2的球棍模型: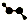 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 电离常数随着弱电解质浓度的增大而增大 | |
| B. | CH3COOH的电离常数表达式为Ka=c(CH3COOH)c(H+)•c(CH3COO−) | |
| C. | 电离常数只受温度影响,与浓度无关 | |
| D. | CH3COOH溶液中加入少量CH3COONa固体,电离常数减小 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 化学反应速率变化时,化学平衡一定发生移动 | |
| B. | 化学平衡发生移动时,化学反应速率一定变化 | |
| C. | 正反应进行的程度越大,正反应速率一定越大 | |
| D. | 使化学反应速率发生变化,而化学平衡不移动的影响因素,一定是催化剂 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2H2(g)+O2(g)=2H2O(g)△H=-286 kJ/mol | B. | 2H2(g)+O2(g)=2H2O(g)△H=-572 kJ/mol | ||
| C. | H2(g)+12O2(g)=H2O(g)△H=-330 kJ/mol | D. | H2O(g)=H2(g)+12O2(g)△H=+242 kJ/mol |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 容器内X、Y、Z的速率之比为1:2:2 | |
| B. | 单位时间生成0.1 mol X的同时生成0.2 mol Z | |
| C. | 容器内X、Y、Z的浓度之比为1:2:2 | |
| D. | 容器内气体密度不随时间变化 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①④ | B. | ②⑤⑥ | C. | ③ | D. | ②④⑦ |
查看答案和解析>>
科目: 来源: 题型:填空题
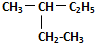 和
和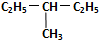 .
.查看答案和解析>>
科目: 来源: 题型:解答题
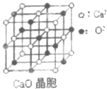 可以由下列反应合成三聚氰胺:CaO+3C高温_CaC2+CO↑,CaC2+N2高温_CaCN2+C,
可以由下列反应合成三聚氰胺:CaO+3C高温_CaC2+CO↑,CaC2+N2高温_CaCN2+C,查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 在氨水中加入少量的水或氯化铵固体后,都能使溶液中的c(NH4+)减小 | |
| B. | 相同体积、pH均为3的HA和HB两种酸分别与足量的锌充分反应,HA放出的氢气多,说明HB的酸性比HA的酸性强 | |
| C. | 工业电解食盐水中,电解池被阳离子交换膜隔成阴极室和阳极室,目的是避免阳极产生的气体与烧碱反应 | |
| D. | 在等浓度的NaCl和Na2CrO4稀溶液中滴加AgNO3溶液,先析出AgCl沉淀,则Ksp(AgCl)<Ksp(Ag2CrO4) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com