
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-硫及其化合物 题型:022
在淀粉KI溶液中加入适量稀硫酸,再滴加少量NaClO溶液,溶液即变蓝色,写出该反应的离子方程式:________.在上述蓝色溶液中滴加足量的Na2SO3溶液,蓝色逐渐消失,写出该反应的离子方程式:________.
从以上实验可知ClO-,I2,SO32-的氧化性由强到弱的顺序是________.
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-离子反应 题型:022
海水中溶解大量的气体物质和各种盐类.人类在陆地上发现的100多种元素,在海水中可以找到80多种.
请回答下列问题:
(1)工业上常用的水处理技术是使用离子交换树脂与水中的离子进行交换.聚丙烯酸钠是一种离子交换树脂,写出聚丙烯酸钠单体的结构简式________.
(2)空气吹出法是目前从海水中提取溴的常用方法,流程如下(苦卤:海水蒸发结晶分离出食盐后的母液):
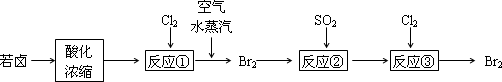
①反应①的离子方程式为___________________;
②反应②的化学方程式为___________________.
(3)苦卤中含有较多的NaCl、MgCl2、KCl、MgSO4等物质.用沉淀法测定苦卤中MgCl2的含量(g/L),测定过程中需要获取的数据有________.
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-离子反应 题型:022
向Ba(OH)2溶液中,逐滴加入明矾溶液至溶液中Ba2+恰好完全沉淀,其反应的离子方程式为:________.
在上述溶液中,继续滴加明矾溶液,请写出此步反应的离子方程式:________.
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-离子反应 题型:022
向Ba(OH)2溶液中,逐滴加入NaHSO4溶液至恰好不再生成沉淀为止,写出反应的离子方程式:________.
在以上溶液中,继续滴加NaHSO4溶液,写出此步反应的离子方程式:________.
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-离子反应 题型:022
向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至中性,写出发生反应的离子方程式:________.
在以上中性溶液中,继续滴加Ba(OH)2溶液,写出此步反应的离子方程式:________.
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-离子反应 题型:022
在淀粉KI溶液中加入适量稀硫酸,再滴加少量NaClO溶液,溶液即变蓝色,写出该反应的离子方程式:________.在上述蓝色溶液中滴加足量的Na2SO3溶液,蓝色逐渐消失,写出该反应的离子方程式:________.
从以上实验可知ClO-,I2,SO32-的氧化性由强到弱的顺序是________.
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-离子反应 题型:022
试列举出三种不同类别的物质(酸、碱、盐)之间的反应,它们对应的离子方程都可用“Ba2++SO42-![]() BaSO4↓”来表示,请写出有关反应的化学方程式(3个)
BaSO4↓”来表示,请写出有关反应的化学方程式(3个)
①______________________;
②______________________;
③______________________.
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-离子反应 题型:022
离子反应是中学化学中重要的反应类型.回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在有________
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)可用图示的方法表示不同反应类型之间的关系.如分解反应和氧化还原反应可表示为下图.请在下面的方框中画出离子反应、置换反应和氧化还原反应三者之间的关系.


(3)离子方程式是重要的化学用语.下列是有关高考资源网离子方程式的一些错误观点,请在下列表格中用相应的“离子方程式”否定这些观点.

(4)已知RxO42-+MnO4-+H+-RO2+Mn2++H2O的变化过程中,有0.2 mol RxO42-离子参加反应时,共转移0.4 mol电子.则x=________;
(5)过二硫酸钾(K2S2O8)具有强氧化性,可将I-氧化为I2:S2O82-+2I-=2SO42-+I2通过改变反应途径,Fe3+、Fe2+均可催化上述反应.试用离子方程式表示Fe3+对上述反应的催化过程.________、________(不必配平).
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-反应热 题型:022
已知a、I、e为三种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下:

物质A由a、e构成,B、C、D、K都是单质,反应①~⑤都是用于工业生产的反应,各有关物质之间的相互反应转化关系如下图所示:
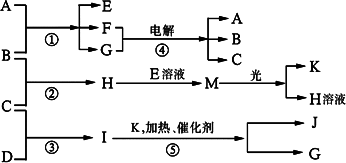
请填写下列空白:?
(1)写出下列物质的化学式:B:________;J:________.
(2)写出下列反应的离子方程式:
①H+E(溶液)→M_________.
②I溶于G________________.
(3)在通常状况下,若1 g C气体在B气体中燃烧生成H气体时放出92.3 kJ热量,则2 mol H气体完全分解生成C气体和B气体的热化学方程式为________.
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编:化学反应速率 题型:022
“温室效应”是全球关注的环境问题之一.CO2是目前大气中含量最高的一种温室气体.因此,控制和治理CO2是解决温室效应的有效途径.
(1)下列措施中,有利于降低大气中CO2浓度的有:________.(多选,填字母)
a.减少化石燃料的使用
b.植树造林,增大植被面积
c.采用节能技术
d.利用太阳能、风能
(2)将CO2转化成有机物可有效实现碳循环.CO2转化成有机物的例子很多,如:
a.6CO2+6H2O![]() C6H12O6
C6H12O6
b.CO2+3H2![]() CH3OH+H2O
CH3OH+H2O
c.CO2+CH4![]() CH3COOH
CH3COOH
d.2CO2+6H2![]() CH2
CH2![]() CH2+4H2O
CH2+4H2O
以上反应中,最节能的是________,原子利用率最高的是________.
(3)文献报道某课题组利用CO2催化氢化制甲烷的研究过程如下:
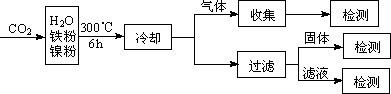
反应结束后,气体中检测到CH4和H2,滤液中检测到HCOOH,固体中检测到镍粉和Fe3O4.
CH4、HCOOH、H2的产量和镍粉用量的关系如下图所示(仅改变镍粉用量,其他条件不变):
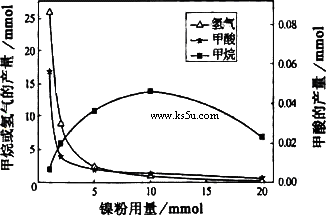
研究人员根据实验结果得出结论:
HCOOH是CO2转化为CH4的中间体,即:CO2![]() HCOOH
HCOOH![]() CH4
CH4
①写出产生H2的反应方程式________.
②由图可知,镍粉是________.(填字母)
A.反应的催化剂
B.反应的催化剂
C.反应的催化剂
D.不是催化剂
③当镍粉用量从1m mol增加到10m mol,反应速率的变化情况是________.(填字母)
a.反应Ⅰ的速率增加,反应Ⅱ的速率不变
b.反应Ⅰ的速率不变,反应Ⅱ的速率增加
c.反应ⅠⅡ的速率均不变
d.反应ⅠⅡ的速率均增加,且反应Ⅰ的速率增加得快
e.反应ⅠⅡ的速率均增加,且反应Ⅱ的速率增加得快
f.反应Ⅰ的速率减小,反应Ⅱ的速率增加
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com