
科目: 来源:江苏省南京市2008届高三质量检测化学试卷 题型:022
工业上由丙烯经下列反应可制得F、G两种高分子化合物,它们都是常用的塑料.
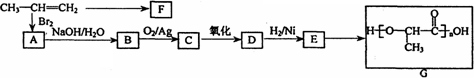
(1)聚合物F的结构简式是________;
(2)D转化为E的化学方程式是________;A转化为B的反应类型是________.
(3)在一定条件下,两分子E能脱去两分子水形成一种六元环状化合物,该化合物的结构简式是________.
(4)E有多种同分异构体,写出3种含有一个羟基、一个酯基的E的同分异构体的结构简式:________、________、________.
(5)已知:①RX+Mg![]() RMgX,
RMgX,
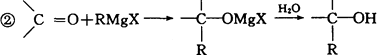
写出丙烯、甲醛等为原料合成![]() 的反应流程图.
的反应流程图.
提示:①合成过程中无机试剂任选;②只选用本题提供的信息和学过的知识;③合成反应流程图表示方法示例如下:由乙醇合成二溴乙烷的反应流程图可表示为CH3CH2OH![]() CH2=CH2
CH2=CH2![]() CH2BrCH2Br
CH2BrCH2Br
查看答案和解析>>
科目: 来源:江苏省南京市2008届高三质量检测化学试卷 题型:022
在一定体积的密闭容器中,进行如下化学反应:
CO(g)+H2O(g)![]() CO2(g)+H2(g),其化学平衡常数K和温度k的关系如下表:
CO2(g)+H2(g),其化学平衡常数K和温度k的关系如下表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=________.该反应为________反应(选填“吸热”、“放热”).
(2)能判断该反应是否达到化学平衡状态的依据是________.
(a)容器中压强不变 (b)混合气体中c(CO)不变
(c)![]() 逆(H2)=
逆(H2)=![]() 正(H2O) (d)c(CO2)=c(CO)
正(H2O) (d)c(CO2)=c(CO)
(3)830℃时,容器中的反应已达到平衡.在其他条件不变的情况下,缩小容器的体积.平衡________移(选填“向正反应方向”、“向逆反应方向”、“不”)
(4)若830℃时,向容器中充入1 mol CO、5 mol H2O,反应达到平衡后,CO的转化率为________.
查看答案和解析>>
科目: 来源:江苏省南京市2008届高三质量检测化学试卷 题型:022
钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”.试回答下列问题:
(1)钛有![]() Ti和
Ti和![]() Ti两种原子,它们互称为________.Ti元素在元素周期表中的位置是第________周期,第________族;基态原子的电子排布式为________;按电子排布Ti元素在元素周期表分区中属于________区元素.
Ti两种原子,它们互称为________.Ti元素在元素周期表中的位置是第________周期,第________族;基态原子的电子排布式为________;按电子排布Ti元素在元素周期表分区中属于________区元素.
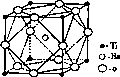
(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构如图所示,它的化学式是________.
(3)现有含Ti3+的配合物,化学式为[TiCl(H2O)5]Cl2·H2O.配离子[TiCl(H2O)5]2+中含有的化学键类型是________,该配合物的配体是________.
查看答案和解析>>
科目: 来源:江苏省淮安中学2008届高三第一次月考化学试卷 题型:022
有一无色透明溶液,欲确定是否含有下列离子:Na+、Mg2+、Al3+、Fe2+、Ba2+、NO![]() 、SO
、SO![]() 、Cl-、I-、HCO
、Cl-、I-、HCO![]() ,取该溶液实验如下:
,取该溶液实验如下:
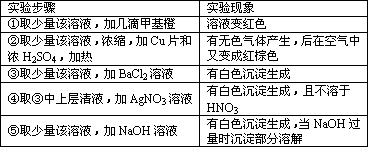
(1)溶液中肯定存在的离子是________________________.
(2)溶液中肯定不存在的离子是________________________.
(3)为进一步确定其他离子,应该补充的实验是________
查看答案和解析>>
科目: 来源:江苏省淮安中学2008届高三第一次月考化学试卷 题型:022
中学化学中几种常见物质的转化关系如下:(提示:A与硫反应生成低价态)将D溶液滴入沸水中可得到以F为分散质的红褐色胶体.请回答下列问题:
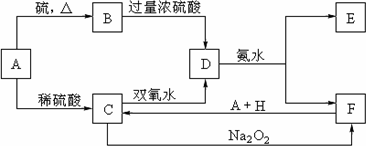
(1)红褐色胶体E粒子直径大小的范围:________.
(2)A、B、H的化学式:A________,B________,H________.
(3)①H2O2分子的电子式:________
②写出C的酸性溶液与双氧水反应的离子方程式:________.
(4)写出鉴定E中阳离子的实验方法和现象:________.
查看答案和解析>>
科目: 来源:江苏省淮安中学2008届高三第一次月考化学试卷 题型:022
KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯.其变化可表述为:
aKClO3+bHCl(浓)——cKCl+dClO2+eCl2↑+fH2O
(1)、浓盐酸在反应中显示出来的性质为________、________;还原产物为(填名称)________.
(2)、根据Cl元素守恒得a、b、c、的关系式为________.
(3)、产生2 mol ClO2,则转移的电子的物质的量为________ mol.
(4)、写出该反应的离子方程式________.
查看答案和解析>>
科目: 来源:2008届高三化学氮族单元测试题 题型:022
NO分子因污染空气而臭名昭著.近年来,发现少量的NO在生物体内许多组织中存在,它有扩张血管、免疫、增强记忆的功能,而成为当前生命科学的研究热点.NO亦被称为“明星分子”,试回答下面问题:
(1)NO对环境的危害在于________.
A.破坏臭氧层
B.高温下能使一些金属被氧化
C.造成酸雨
D.与人体血红蛋白结合
(2)在含Cu+离子酶活化中心中,亚硝酸根离子可转化为NO,写出Cu+和亚硝根离子在酸性水溶液中反应的离子方程式________.
(3)在常温下,将NO气体压缩到1.01×107 PA,在一个体积固定的容器里加热到50℃.发现气体的压强迅速下降,压强降至略小于原压强2/3就不再改变,已知其中一种产物为N2O,写出上述变化的化学方程式________.
(4)解释(3)中为什么最后的气体总压强小于原压强的2/3?
___________________
查看答案和解析>>
科目: 来源:深圳外国语学校2008届高三年级第二次质量检测化学试题 题型:022
为节省药品和时间,甲乙丙三位同学用铜片、锌片、稀硫酸、硫酸铜溶液、直流电源、石墨电极、导线、烧杯、试管等中学化学常见的药品和仪器,进行巧妙的构思,以“接力”的方式,设计了比较铜与锌的金属活动性相对强弱的系列实验.试回答下列问题:
(1)甲同学分别将一小片铜片、锌片置于烧杯底部(铜锌不接触),小心向烧杯中加入稀硫酸,观察到的现象是________.甲同学的设计方案的理论依据是________________________________.
(2)乙同学接着甲同学的实验,向烧杯中加________溶液,进而观察到的现象是________.乙同学判断铜锌金属活动性相对强弱的理论依据是________.
(3)丙同学使用直流电源和石墨电极组装好电极装置,向乙同学实验后的溶液中补充了必要的试剂(作电解液).反应在调控下随时发生,实验中有关电解反应的化学方程式为________________;观察到的明显实验现象是________________.
(4)请你再单独设计一个简单的实验(试剂、仪器任选),探究和证实锌和铜金属活动性的相对强弱(简要说明实验操作)________________________
查看答案和解析>>
科目: 来源:深圳外国语学校2008届高三年级第二次质量检测化学试题 题型:022
下图表示一些常见物质间的相互转换关系,其中C、E都是金属单质,常温下H为无色液体,C与B的稀溶液不反应,B与K是同一类别的物质,在无色灯焰中灼烧F和L时火焰均为黄色.将新制M的悬浊液与病人尿液共热,能诊断病人是否患有糖尿病.试回答:
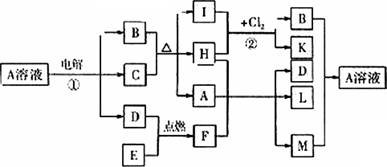
(1)F的电子式为________;反应①的阳极反应式为________.
(2)反应②的化学方程式为________.
(3)B溶液与M反应的离子方程式为________.
(4)I与F有一项相同的用途是________.
(5)新制M的悬浊液与葡萄糖共热至沸腾,发生反应的化学方程式为________.
查看答案和解析>>
科目: 来源:山西省实验中学2008届高三年级第一次月考化学试题 题型:022
如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
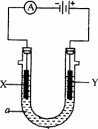
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为________.
在X极附近观察到的现象是________.
②Y电极上的电极反应式为________.
检验该电极反应产物的方法是________.
(2)如果要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是________,电极反应式是________.
②Y电极的材料是________,电极反应式是________.
(说明:杂质发生的电极反应不必写出)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com