
科目: 来源:江苏省无锡市2009届高三上学期模拟考试、化学 题型:022
已知A、B、C、D、E都是元素周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.B原子的p轨道半充满,形成的氢化物的沸点是同主族元素的氢化物中最低的.D原子得到一个电子后3p轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为26,E原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C、D的第一电离能由小到大的顺序为________.
(2)C的氢化物分子是________(填“极性”或“非极性”)分子.
(3)化合物BD3的分子空间构型是________.
(4)E元素原子的核外电子排布式是________;E的一种常见配合物E(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂.据此可判断E(CO)5的晶体类型为________;E(CO)5中的配体CO与N2、CN-等互为等电子体,写出CO分子的结构式________.
(5)金属E单质的晶体在不同温度下有两种堆积方式,晶胞分别如图所示.体心立方晶胞和面心立方晶胞中实际含有的E原子个数之比为________.

查看答案和解析>>
科目: 来源:江苏省无锡市2009届高三上学期模拟考试、化学 题型:022
苯佐卡因是一种局部麻醉剂,可用于粘膜溃疡、创面等的镇痛,一般制成软膏或栓剂使用,它的工业合成有如下所示的两种途径.途径Ⅰ已逐渐淘汰,现在使用较多的是途径Ⅱ.

已知:①当苯环上连有甲基时,再引入的其他基团主要进入它的邻位或对位;当苯环上连有羧基时,再引入的其他基团主要进入它的间位.
②苯胺(![]() )分子中的氨基易被氧化.
)分子中的氨基易被氧化.
请回答下列问题:
(1)反应①的反应类型为________,化合物B的结构简式为________.
(2)反应⑦的化学方程式为________________.
(3)下列关于上述合成路线的说法正确的是________.
a.反应①除了主要生成A物质外,还可能生成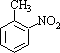 、
、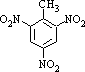 等
等
b.途径Ⅱ中的步骤①和⑤可以互换
c.反应③的另一产物是H2O
d.与途径Ⅱ相比,途经Ⅰ的缺点是步骤多,产率低
e.途经Ⅰ中的步骤③的目的是保护氨基不被步骤④中的酸性高锰酸钾溶液氧化
(4)途经Ⅱ中的步骤⑤和⑥能否互换,说明理由:________________.
(5)苯佐卡因有多种同分异构体.其中有两个对位取代基,-NH2直接连在苯环上,分子结构中含有酯基的同分异构体有:
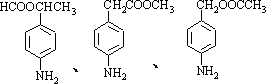 ________、________.
________、________.
查看答案和解析>>
科目: 来源:江苏省无锡市2009届高三上学期模拟考试、化学 题型:022
已探明我国锰矿储量占世界第三位,但富矿仅占6.4%,每年尚需进口大量锰矿石.有人设计了把我国的贫菱锰矿(MnCO3含量较低)转化为高品位“菱锰矿砂”(MnCO3含量高)的绿色工艺.该工艺流程如下图所示:
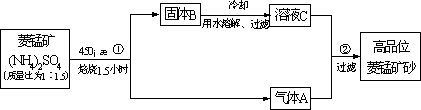
已知焙烧反应①的化学方程式:(NH4)2SO4+MnCO3![]() MnSO4+2NH3↑+CO2↑+H2O.
MnSO4+2NH3↑+CO2↑+H2O.
(1)写出反应②的离子方程式________.
(2)上述工艺流程中,可以循环利用的物质有(NH4)2SO4、________、________.从物料平衡角度看,理论上生产过程中________(填“需要”或者“不需要”)添加(NH4)2SO4.
(3)向物质的量浓度均为0.01 mol·L-1的MnSO4和BaCl2混合溶液中,滴加Na2CO3溶液,先沉淀的是________(填离子符号);当两种沉淀共存时,溶液中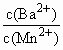 =________.
=________.
查看答案和解析>>
科目: 来源:江苏省溧阳市南渡高级中学2009届高三模拟考试(化学) 题型:022
下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.
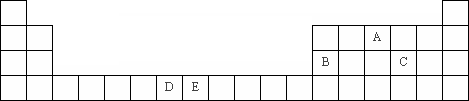
试回答下列问题:
(1)请写出元素D的基态原子电子排布式________;
(2)D、E两元素的部分电离能数据列于下表:
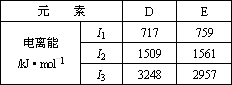
比较两元素的I2、I3可知,气态D2+再失去一个电子比气态E2+再失去一个电子难.对此,你的解释是________;
(3)A的氢化物的中心原子的杂化形式为________;C在空气中燃烧产物的分子构型为________,与其互为等电子体的单质的分子式为________.
(4)B单质晶体中原子的堆积方式如图甲所示,其晶胞特征如右图乙所示,原子之间相互位置关系的平面图如图丙所示.晶胞中B原子的配位数为________,一个晶胞中B原子的数目为________.
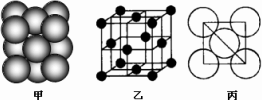
查看答案和解析>>
科目: 来源:江苏省溧阳市南渡高级中学2009届高三模拟考试(化学) 题型:022
请仔细观察两种电池的构造示意图,回答下列问题:
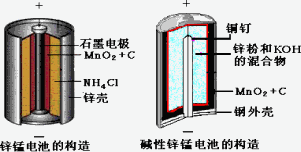
(1)碱性锌锰电池的总反应式:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,则负极的电极反应式:________
(2)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大.试从影响反应速率的因素分析其原因是________
(3)某工厂回收废旧锌锰电池,其工艺流程如下:
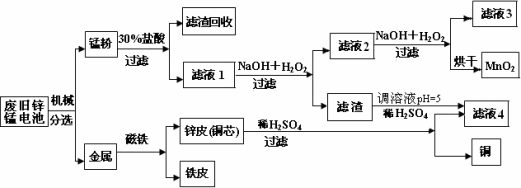
已知:生成氢氧化物的pH如下表:

①经测定,“锰粉”中除含少量铁盐和亚铁盐外,主要成分应是MnO2、Zn(OH)2________.
②第一次加入H2O2后,调节pH=8.0.目的是________.
③试列举滤液4的应用实例________.
查看答案和解析>>
科目: 来源:江苏省溧阳市南渡高级中学2009届高三模拟考试(化学) 题型:022
阿司匹林能迅速解热、镇痛.长效缓释阿司匹林可在体内逐步水解而疗效更佳.用丙酮为主要原料合成长效缓释阿司匹林的流程如下图.
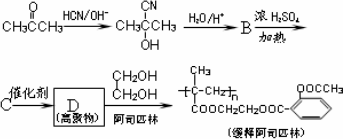
回答下列问题:
(1)上述合成C的路线曾用作有机玻璃单体(CH2=![]() -COOCH3)合成路线的一部分.现在人们利用最新开发的+2价钯的均相钯催化剂体系,将丙炔在甲醇和一氧化碳存在下,于60℃、6 MPa条件下羰基化,一步制得CH2=
-COOCH3)合成路线的一部分.现在人们利用最新开发的+2价钯的均相钯催化剂体系,将丙炔在甲醇和一氧化碳存在下,于60℃、6 MPa条件下羰基化,一步制得CH2=![]() -COOCH3,其化学方程式为:________.
-COOCH3,其化学方程式为:________.
如此改进的优点为:________.
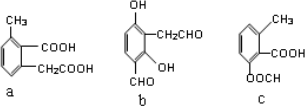
(2)阿司匹林的结构简式为________,下列物质与阿司匹林互为同分异构体的有________(填字母编号).
(3)根据题示信息,用苯酚为主要原料合成![]() ,模仿以上流程图设计合成路线,标明每一步的反应物及反应条件.(有机物写结构简式,其它原料自选)
,模仿以上流程图设计合成路线,标明每一步的反应物及反应条件.(有机物写结构简式,其它原料自选)
例:由乙醇合成聚乙烯的反应流程图可表示为
CH3CH2OH![]() CH2=CH2
CH2=CH2![]()
![]() CH2-CH2
CH2-CH2![]()
查看答案和解析>>
科目: 来源:江苏省溧阳市南渡高级中学2009届高三模拟考试(化学) 题型:022
A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素.在一定条件下相互转化的关系如下图所示(部分反应中的H2O已略去).请按要求回答下列问题:
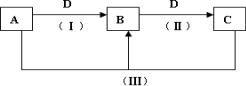
(1)若D为金属单质,且D是用量最大、用途最广的金属,若加热蒸干B的溶液没有得到B的盐,则B的化学式可能为________.
(2)A常用作制冷剂,B和D为空气的主要成分,则反应(Ⅲ)的化学方程式为________.
(3)D为氯碱工业的重要产品,反应(Ⅲ)的离子方程式可以是________.
(4)D为酸或酸性气体,则A、B、C、D可以是________(请按顺序写出合理任意一组物质的化学式即可).
查看答案和解析>>
科目: 来源:江苏省溧阳市南渡高级中学2009届高三模拟考试(化学) 题型:022
北京时间2008年2月21日上午11时26分,美国用导弹击毁了失控的卫星.美方称,卫星坠落地面时,燃料罐中装有的约453 kg联氨(N2H4),可能发生泄漏,造成伤害.
(1)联氨是一种无色可燃的液体,溶于水显碱性,其原理与氨相似,但其碱性不如氨强,写出其溶于水呈碱性的离子方程式:________.
(2)联氨(N2H4)是航天飞船常用的高能燃料.联氨可用氨和次氯酸钠按一定物质的量之比混合反应生成联氨、氯化钠和水;该反应的氧化产物是________.也可以采用尿素[CO(NH2)2]为原料制取,方法是在高锰酸钾催化剂存在下,尿素和次氯酸钠、氢氧化钠溶液反应生成联氨、另外两种盐和水,写出其反应的化学方程式________.
(3)火箭推进器中分别装有联氨和过氧化氢,当它们混合时即产生气体,并放出大量热.已知:12.8 g液态联氨与足量过氧化氢反应生成氮气和水蒸气,放出256.65 kJ的热量;
H2O(l)=H2O (g) D H=+44 kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g) D H=-196.4 kJ·mol-1
则写出表示联氨燃烧热的热化学方程式为________.
查看答案和解析>>
科目: 来源:江苏省金坛市第一中学2009届高三化学综合模拟 题型:022
A-J是中学化学中常见的物质,它们之间的转化关系如下框图所示(部分产物已略去).已知A是一种高熔点物质,J是一种红褐色沉淀.
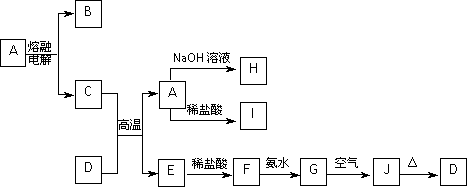
请回答下列问题:
(1)A的化学式为________.
(2)H溶液中通入过量的CO2,其反应的离子方程式是________________.G→J的化学方程式为________________.
(3)D物质恰好溶于一定量的稀盐酸后,用合适的化学用语表示所得溶液显酸性的原因________________________.
(4)现有一定量C、E混合物与稀HNO3充分反应,反应过程中无任何气体放出.在反应结束后的溶液中,逐滴加入4 mol/L NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示.坐标图c点溶液中溶质除C和E的硝酸盐外,还含有的溶质是___________________________,
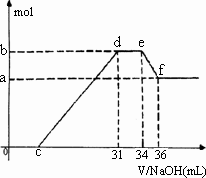
查看答案和解析>>
科目: 来源:江苏省金坛市第一中学2009届高三化学综合模拟 题型:022
下图所示各物质是由1~20号元素中部分元素组成的单质或其化合物,图中部分反应条件未列出.已知C、H是无色有刺激性气味的气体,D是一种黄绿色的气体单质,物质J可用于饮水消毒.反应②和④是化工生产中的重要反应,反应⑤是实验室制备气体C的重要方法.
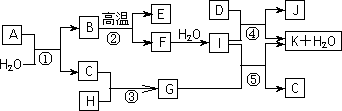
请回答下列问题:
(1)物质E的电子式是________;物质J的名称为________.
(2)反应⑤的化学方程式为__________________________________.
(3)反应③的现象为________________________________________.
(4)物质A由三种元素组成,1 mol A与水反应可生成1 mol B和2 mol C,A的化学式为________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com